Actividades
Actividades
1 Reacciones químicas
1 Reacciones químicas
Ajusta en tu cuaderno estas ecuaciones químicas:
- Zn(s) + HCl(ac) → ZnCl2(ac) + H2(g)
- C2H6(g) + O2(g) → CO2(g) + H2O(ac)
- Al(s) + O2(g) → Al2O3(s)
- NO2(g) → N2O4(g)
¿Cuáles son los coeficientes necesarios para que la reacción de combustión del benceno esté ajustada?
C6H6(l) + O2(g) → CO2(g) + H2O(l)
- 1; 15 → 6; 3
- 1; 7 → 3; 3
- 2; 15 → 12; 6
- 2; 7,5 → 6; 6
Ajusta las siguientes ecuaciones químicas:
- CaCl2(ac) + AgNO3(ac) → Ca(NO3) 2(ac) + AgCl(s)
- N2(g) + H2(g) → NH3(g)
- H2SO4(l) + KNO3(l) → K2SO4(l) + HNO3(l)
- NH3(g) + O2(g) → NO(g) + H2O(g)
2 Leyes de las reacciones químicas
2 Leyes de las reacciones químicas
Ley de la conservación de la masa
Ley de la conservación de la masa
El científico Robert Boyle calcinó un metal durante horas en un recipiente abierto y observó que la masa había aumentado.
- ¿Contradice la ley de conservación de la masa? ¿Qué pasó?
- ¿Se obtendría igual resultado si esa misma reacción se realizase en un recipiente cerrado?
+ Se hace reaccionar cobre y azufre en un tubo cerrado y se obtienen los siguientes datos:

- ¿Cuál era la masa de las sustancias antes de que se produjera la reacción?
- ¿Cuánto ha cambiado la masa de las sustancias?
- ¿Crees que se ha cumplido la ley de Lavoisier?
- ¿A qué se debe el cambio de masa experimentado?
Leyes de los volúmenes de combinación
Leyes de los volúmenes de combinación
Se observa que, en una reacción química, 10 L de nitrógeno, N2, reaccionan con 30 L de hidrógeno, H2, y se forman 20 L de amoniaco, NH3.
- Escribe la ecuación química correspondiente a este proceso.
- Enuncia la ley que responde a los datos del enunciado.
- Si al mismo volumen inicial de nitrógeno se le añaden 40 L de hidrógeno, ¿cuánto amoniaco se formará?
Escribe en tu cuaderno, según la ley de Avogadro, la siguiente ecuación química, que aparece expresada de acuerdo con la ley de Gay-Lussac:
3 volúmenes de hidrógeno + 1 volumen de nitrógeno →
→ 2 volúmenes de amoniaco
A 110 ºC se mezclan 4 L de hidrógeno, H2, con 2 L de oxígeno, O2, para formar vapor de agua, H2O.
- Escribe la ecuación ajustada que exprese la formación del agua.
- ¿Cuántos litros de vapor de agua se formarán?
- ¿Qué ley se ha cumplido?
3 Clasificación de las reacciones químicas
3 Clasificación de las reacciones químicas
Según el producto que se obtiene
Según el producto que se obtiene
Escribe en tu cuaderno qué tipo de reacción ocurre en cada caso.

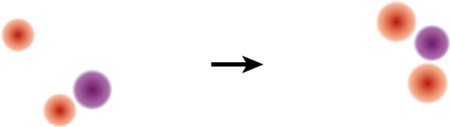

La reacción que representa la ecuación química siguiente ¿es de sustitución? Razona la respuesta.
2KI(ac) + Pb(NO3)2(ac) → PbI2(s) + 2KNO3(ac)
+ Clasifica las siguientes ecuaciones según el producto que se obtiene:
- Zn(s) + CuSO4(ac) → ZnSO4(ac) + Cu(s)
- CaO(s) + CO2(g) → CaCO3(s)
- 2KClO3(s) → 2KCl(s) + 3O2(g)
- N2O4(g) → 2NO2(g)
- 2NH3(g) → N2(g) + 3H2(g)
- Zn(s) + 2HBr(ac) → ZnBr2(ac) + H2(g)
- C(s) + O2(g) → CO2(g)
- 2H2(g) + O2(g) → 2H2O(g)
- H2CO3(ac) → CO2(g) + H2O(l)
- Ca(OH)2(ac) + 2HCl(ac) → CaCl2(s) + 2H2O(l)
¿Cuál de las siguientes ecuaciones corresponde a una reacción de sustitución?
- PCl5 (g) → PCl2(g) + Cl2(g)
- Br2(g) + 2KI(ac) → I2(s) + 2KBr(ac)
- CaO(s) + H2O(l) → Ca(OH)2(s)
- 2HgO(l) → 2Hg(l) + O2(g)
Según la velocidad de la reacción
Según la velocidad de la reacción
¿Por qué las reacciones entre gases son más rápidas que entre sólidos? ¿Por qué la concentración de los reactivos aumenta la velocidad de una reacción química?
Una piedra caliza reacciona con ácido clorhídrico produciendo dióxido de carbono, entre otras sustancias. ¿En qué caso se observará un mayor desprendimiento de burbujas: cuando la piedra caliza se encuentra en una sola pieza o si está triturada? Justifica tu respuesta.
¿Por qué se guardan los alimentos en el frigorífico?
¿Qué es un antioxidante alimentario?

+ Al quemar un terrón de azúcar o sacarosa, reacciona con el oxígeno y se produce dióxido de carbono. Ahora bien, al acercar un mechero, el azúcar se carameliza y no arde; sin embargo, si se le echa un poco de ceniza encima, el azúcar arde con llama. ¿Puedes explicar por qué sucede esto?
Según la energía intercambiada
Según la energía intercambiada
Define los conceptos de reacción endotérmica y reacción exotérmica y deduce a qué tipo corresponde cada uno de los diagramas de energía siguientes:
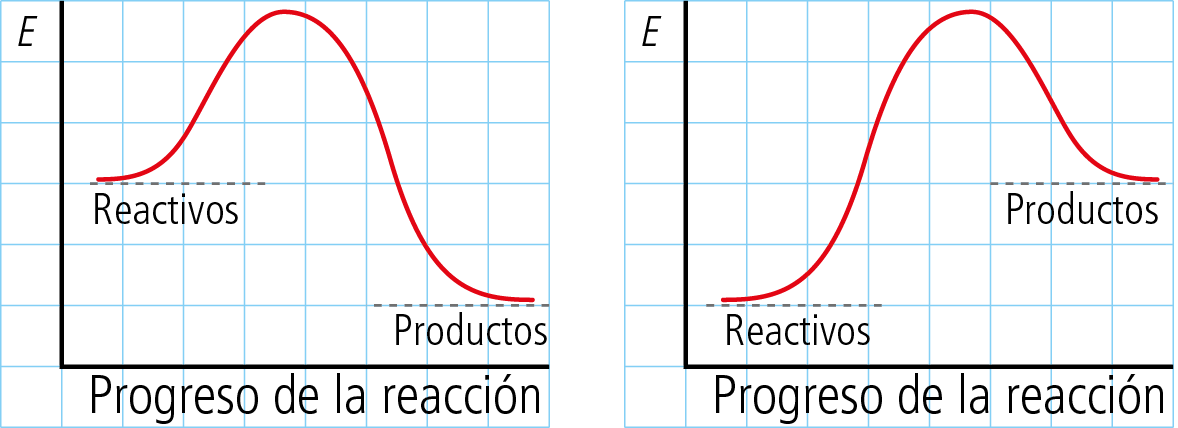
Comentarios