- Obtener enlace
- X
- Correo electrónico
- Otras aplicaciones
02 Leyes de las reacciones químicas
La formulación de la ley de la conservación de la masa dio inicio al estudio de las leyes ponderales, que indican cuáles son las masas de las sustancias que intervienen en cada reacción química.
2.1 LEY DE LA CONSERVACIÓN DE LA MASA
2.1 LEY DE LA CONSERVACIÓN DE LA MASA
El químico francés Antoine Lavoisier (1743-1794) realizó un experimento en el que calcinó estaño en un recipiente cerrado y observó que, tras el proceso, la masa total no variaba.
Comprobación de la ley de Lavoisier
Comprobación de la ley de Lavoisier
Se pesan 20 g de ácido clorhídrico diluido (HCl) y se vierten en un Erlenmeyer.
Se pesan 10 g de carbonato ácido de sodio (NaHCO3) y se vierten en un globo.
Se ajusta la boca del globo a la boca del Erlenmeyer manteniendo separadas las dos sustancias.
Se da la vuelta al globo de modo que todo el carbonato ácido de sodio caiga en el Erlenmeyer para que reaccione:
HCl(ac) + NaHCO3(s) → NaCl(ac) + H2O(l) + CO2(g)
Sin soltar el globo, se pesa la mezcla tras la reacción. Se observa que no hay cambio en la masa total de las sustancias.

En 1789, Lavoisier enunció la ley de la conservación de la masa:
La ley de la conservación de la masa o ley de Lavoisier indica que, en toda reacción química, la masa de las sustancias que reaccionan es igual a la masa de las sustancias resultantes.
Recuerda
Recuerda
Masa atómica del H = 1 u y masa atómica del Cl = 35,5 u
Por ejemplo, para que la reacción que tiene lugar entre el hidrógeno, H2, y el cloro, Cl2, para dar ácido clorhídrico, HCl, cumpla la ley de Lavoisier, hay que ajustarla. Así la suma de las masas de los reactivos es igual a la masa del producto:
H2 (g) + Cl2(g) → 2HCl(ac)
2 u 71 u 2 · 36,5 u = 73 u
La ley de la conservación de la masa se puede explicar a través de la teoría de las colisiones. En una reacción química, solo cambia la forma de organizarse los átomos. Como el número de cada tipo de átomos sigue siendo el mismo en los reactivos y en los productos, la masa total se conserva.
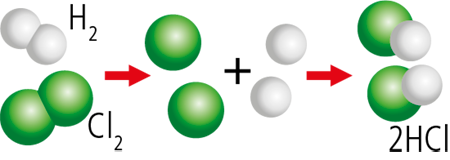
Hay el mismo número de átomos de H y Cl en ambos lados de la ecuación.
Reactivo en exceso
Reactivo en exceso
Puede suceder que las cantidades de algunos de los reactivos se encuentren en exceso; en ese caso, la reacción se detiene cuando se termina el reactivo que está en menor proporción.
2.2 LEYES DE LOS VOLÚMENES DE COMBINACIÓN
2.2 LEYES DE LOS VOLÚMENES DE COMBINACIÓN
Recuerda
Recuerda
En 1808, John Dalton enunció su teoría atómica, que se basaba en la ley de la conservación de la masa, según la cual la materia estaba formada por átomos. Dalton sostuvo que había átomos de elementos y átomos de compuestos, ya que desconocía la existencia de las moléculas.
Según Dalton, la reacción para formar agua se producía así:
H + O → HO
1 átomo + 1 átomo → 1 átomo
Esta relación no explicaba los resultados obtenidos por los experimentos de Gay Lussac:
2 vols. H + 1 vol. O → 2 vols. H2O
El químico francés Louis J. Gay-Lussac (1778-1850) midió, en las mismas condiciones de presión y temperatura, los volúmenes de todos los gases implicados en una reacción.
Gay-Lussac hizo reaccionar a alta temperatura hidrógeno y oxígeno para formar vapor de agua. Comprobó entonces que:
2H2(g) + O2(g) → 2H2O(g)
2 volúmenes de hidrógeno + 1 volumen de oxígeno → 2 volúmenes de agua
Con estos resultados, Gay-Lussac enunció la ley de los volúmenes de combinación:
En una reacción química, el volumen de gas que reacciona y el volumen de gas resultante guardan una proporción de números enteros sencillos, siempre que se midan en iguales condiciones de presión y temperatura.
Por aquel entonces, esta ley no se podía explicar con la teoría atómica de Dalton, que solo suponía la existencia de átomos. Sin embargo, en 1814, el químico italiano Amedeo Avogadro (1776-1856) consiguió explicar la ley de Gay-Lussac enunciando una hipótesis que lleva su nombre, formada por dos postulados:
En las mismas condiciones de presión y temperatura, volúmenes iguales de gases diferentes contienen el mismo número de partículas.
Las partículas de los elementos gaseosos no son átomos, sino agregados de dos o más átomos denominados moléculas.
De esta forma, los resultados obtenidos por Gay-Lussac en sus experimentos encontraron explicación:
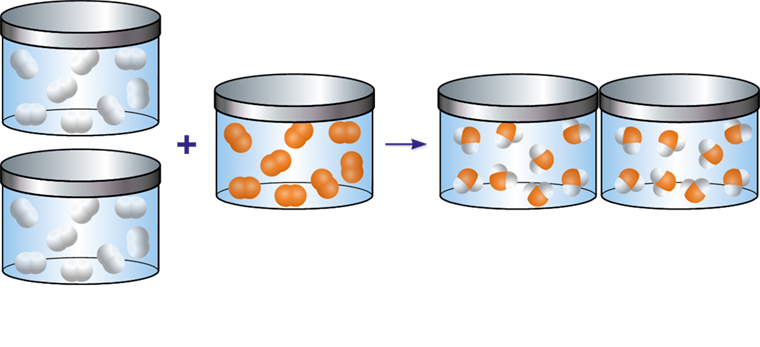
La hipótesis de Avogadro también puede enunciarse de manera inversa:
En idénticas condiciones de presión y temperatura, un determinado número de moléculas de dos gases diferentes ocupan el mismo volumen.
Actividades resueltas
Actividades resueltas
Ajusta estas reacciones químicas:
- I2 + Fe → FeI3
- PdCl2 + HNO3 → Pd(NO3)2 + HCl
- Na2O2 + H2O → NaOH + O2
- Se ajusta, en primer lugar, aquel elemento que varía de número de reactivos a productos, el I. Hay 2 átomos de I en reactivos y 3 átomos de I en productos, por lo que es preciso poner un 3 en I2 y un 2 en FeI3:
3I2 + Fe → 2FeI3
- Ahora se debe ajustar el Fe. Hay 1 átomo de Fe en reactivos y 2 átomos en productos; se ha de poner 2Fe en reactivos:
3I2 + 2Fe → 2FeI3
- Se comprueba que estén todos los átomos ajustados.
- Se ajusta, en primer lugar, aquel elemento que varía de número de reactivos a productos, el I. Hay 2 átomos de I en reactivos y 3 átomos de I en productos, por lo que es preciso poner un 3 en I2 y un 2 en FeI3:
- El número de átomos de Pd en ambos miembros de la reacción está ajustado; de este modo, se ajusta el Cl. Hay 2 átomos de Cl en reactivos y 1 átomo de Cl en productos, por lo que se pone un 2 en HCl:
PdCl2 + HNO3 → Pd(NO3)2 + 2HCl
- Al ajustar el Cl, el número de átomos de H en reactivos y productos no coincide, razón por la que habría que poner un 2 en HNO3:
PdCl2 + 2HNO3 → Pd(NO3)2 + 2HCl
Se comprueba que la ecuación química está ajustada.
- El número de átomos de Pd en ambos miembros de la reacción está ajustado; de este modo, se ajusta el Cl. Hay 2 átomos de Cl en reactivos y 1 átomo de Cl en productos, por lo que se pone un 2 en HCl:
- Se ajustan los elementos distintos de O y H, en este caso el Na. Como hay 2 átomos de Na en reactivos, tiene que haber 2 átomos de Na en productos:
Na2O2 + H2O → 2NaOH + O2
- Se comprueban los H; dado que hay 2 átomos de H en reactivos y 2 en productos, se constata que están ajustados: se han ajustado al ajustar el Na.
- Se comprueban los O en ambos miembros de la ecuación. En reactivos hay 3 átomos de O y en productos 4 átomos de O. Para poder ajustar, hay que poner un 2 en H2O y ajustar de nuevo el NaOH y el Na2O2:
Na2O2 + 2H2O → 2NaOH + O2
- Ahora hay que ajustar los átomos de H y Na. Habría que poner un 4 en NaOH y un 2 en Na2O2 y, por último, verificar que está todo ajustado:
2Na2O2 + 2H2O → 4NaOH + O2
- Se ajustan los elementos distintos de O y H, en este caso el Na. Como hay 2 átomos de Na en reactivos, tiene que haber 2 átomos de Na en productos:
Se calientan 45 g de plomo con 15 g de azufre. Si la relación entre mPb y mS es de 6,5, ¿cuánto sulfuro de plomo(II), PbS, se formará? ¿Sobrará plomo? ¿Sobrará azufre?
Según la ley de las proporciones definidas o de Proust, se cumple que, cuando dos o más elementos se unen para formar un determinado compuesto, lo hacen en una proporción de masas constante, independientemente de las masas iniciales. Es decir:
La masa de azufre que reacciona con los 45 g de plomo es:
La masa de sulfuro de plomo formado es:
Sobran: 15 g – 6,92 g = 8,08 g de azufre
Escribe, según la ley de Avogadro, la siguiente reacción química, expresada de acuerdo con la ley de Gay-Lussac:
1 volumen de hidrógeno + 1 volumen de cloro →
→ 2 volúmenes de cloruro de hidrógeno
Las partículas gaseosas están formadas por moléculas de hidrógeno, de cloro y dos de cloruro de hidrógeno. Así pues:
H2(g) + Cl2(g) → 2HCl(g)
A altas temperaturas, el nitrógeno reacciona con el oxígeno para dar óxido de nitrógeno (NO). Escribe:
- La reacción química según Dalton.
- Aplicando la ley de Avogradro, la reacción química que tiene lugar, si la proporción de volúmenes según Gay-Lussac es:
1 volumen de N + 1 volumen de O →
→ 2 volúmenes de NO
- Según Dalton, las sustancias se encontraban en forma de átomos:
N + O → NO
1 átomo de N + 1 átomo de O → 1 átomo de NO
- Según Gay-Lussac:
1 vol. de nitrógeno + 1 vol. de oxígeno →
→ 2 vols. de óxido de nitrógeno
Para explicar la relación de volúmenes, hay que partir de la existencia de moléculas:
N2(g) + O2(g) → 2NO(g)
- Obtener enlace
- X
- Correo electrónico
- Otras aplicaciones
Comentarios