Experimentación
Reacciones químicas importantes
Reacciones de oxidación-reducción
Reacciones de oxidación-reducción
Escribe en tu cuaderno la ecuación de oxidación del calcio y la de reducción del óxido de cinc, ZnO. Indica qué sustancia es el oxidante y cuál el reductor.
Copia y completa en tu cuaderno las siguientes reacciones de oxidación-reducción:
- 2HgO(l) →
- C(s) + O2(g) →
- Na(s) + O2(g) →
Reacciones de combustión
Reacciones de combustión
Escribe la ecuación de combustión ajustada del gas butano, C4H10, y realiza su ajuste por el método por tanteo.
Cuando el carbono reacciona con poco oxígeno, se formamonóxido de carbono. En cambio, cuando lo hace con exceso de oxígeno, se forma dióxido de carbono. Escribe las ecuaciones de combustión correspondientes a ambos procesos.
En la combustión de 46 g de etanol se desprenden 1 370 kJ. Calcula qué cantidad de calor se liberará cuando se quemen:
- 100 g
- 250 g
- 1 kg
+ Escribe las ecuaciones que representan la oxidación de la plata y la combustión del gas propano, C3H8. ¿Qué tienen en común? ¿En qué se diferencian?
Reacciones ácido-base
Reacciones ácido-base
Clasifica las siguientes sustancias en ácidos y bases y escribe sus ecuaciones de disociación: KOH, HI, Mg(OH)2, LiOH, HNO3, CH3 — COOH, NH4OH, HClO4.
Escribe en tu cuaderno las ecuaciones de disociación de los ácidos HNO3, HBr y H2CO3.
Escribe en tu cuaderno las ecuaciones de disociación de estas bases: NaOH, Cu(OH)2 y Al(OH)3
Escribe en tu cuaderno las siguientes reacciones de neutralización:
- Ácido bromhídrico con hidróxido de calcio.
- Ácido sulfúrico con hidróxido de potasio.
- Ácido nítrico con hidróxido de magnesio.
- Ácido clorhídrico con hidróxido de aluminio.
Indica qué carácter (ácido, básico o neutro) tendrá una disolución cuyo pH es:
- pH = 8
- pH = 4
Escribe las ecuaciones ajustadas de la reacción entre el ácido nítrico, HNO3, y el hidróxido de calcio, Ca(OH)2, y entre el ácido sulfúrico, H2SO4, y el hidróxido de potasio, KOH. ¿Cómo se llaman estas reacciones?
El vinagre es una disolución de ácido acético. ¿Cómo será su pH?
- pH > 7
- pH > 8
- pH = 14
- pH < 7
5 Cantidad de sustancia
5 Cantidad de sustancia
Marca en tu cuaderno la respuesta correcta. En 4 mol de metano, CH4, hay:
- 20 moléculas
- 2,408 8 · 1024 moléculas
- 6,022 · 1023 moléculas
- 20 · 1023 moléculas
Calcula en tu cuaderno las siguientes cantidades:
- La masa molar de la glucosa, C6H12O6.
- La cantidad de sustancia que hay en 315 g de HNO3.
Masas molares: C = 12 g/mol; H = 1 g/mol; O = 16 g/mol; N = 14 g/mol
Copia y completa en tu cuaderno esta tabla:
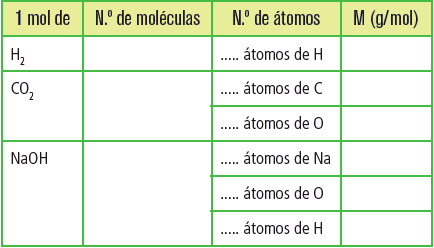
Masas molares: C = 12 g/mol; H = 1 g/mol; O = 16 g/mol; Na = 23 g/mol
Calcula la cantidad de sustancia que hay en 200 g de las siguientes especies:
- Agua, H2O
- Amoniaco, NH3
- Cloruro de sodio, NaCl
Masas molares: H = 1 g/mol; O = 16 g/mol; N = 14 g/mol; Na = 23 g/mol; Cl = 35,5 g/mol
Se dispone de 85 g de amoniaco, NH3. Calcula:
- La cantidad de sustancia.
- El número de moléculas que contiene.
- El número de átomos de nitrógeno.
- El número de átomos de hidrógeno.
Masas molares: H = 1 g/mol; N = 14 g/mol
+ Se dispone de 176 g de dióxido de carbono, CO2, y se desea averiguar:
- La masa molar del CO2.
- La cantidad de sustancia.
- El número de moléculas que contiene.
- El número de átomos de carbono.
- El número de átomos de oxígeno.
- El volumen de CO2, medido en condiciones estándar de presión, 105 Pa, y temperatura, 0 ºC.
Masas molares: C = 12 g/mol; O = 16 g/mol
Se dispone de 160 g de trióxido de azufre, SO3. Contesta razonadamente a estas cuestiones:
- ¿Cuál es la cantidad de sustancia?
- ¿Qué volumen ocupará en condiciones estándar?
- ¿Cuántas moléculas contiene?
- ¿Cuántos átomos de azufre y cuántos de oxígeno hay?
Masas molares: S = 32 g/mol; O = 16 g/mol

Comentarios